Katalysator-Unterstützung: Ein Leitfaden für Materialien und ihre Verwendung
Was ist Catalyst Support?
Die in industriellen Anwendungen verwendeten aktiven Chemikalien wie Platin, Palladium und Rhodium sind sehr teuer. Werden diese aktiven Metalle in loser Schüttung in einen Reaktor eingebracht, neigen sie dazu, zu größeren Katalysatorteilchen zu agglomerieren. Dadurch wird die Reaktionsgeschwindigkeit verringert, was zu einem Verlust an aktiver Substanz führt.
Ein Katalysatorträger ist ein festes, hochporöses Material, das so konzipiert ist, dass es eine große physikalische Fläche bietet, auf der diese aktiven Komponenten (Metall-Nanopartikel bis hin zu einem einzelnen Oberflächenatom) verteilt werden können. Durch die Verankerung dieser aktiven Komponenten schaffen und erhalten die Träger die physikalische Trennung der Metallpartikel. Das feste Trägermaterial bestimmt auch die Form des Katalysators, z. B. Pellets, Extrudate und Kugeln, so dass der Katalysator in großtechnische Reaktoren eingebracht werden kann, ohne dass es zu großen Druckabfällen im Flüssigkeitsstrom kommt, wodurch ein geringer Druckabfall aufrechterhalten wird.
Um die Anforderungen an einen Träger zu verstehen, ist es wichtig, die Katalyse in zwei Hauptmethoden oder -typen zu unterteilen: homogene und heterogene Katalyse.
Homogene Katalyse
Der Katalysator befindet sich in der gleichen Phase wie die Reaktanten und bildet oft eine homogene Lösung. Der Katalysator ist schwieriger aus dem Reaktionsgemisch abzutrennen und erfordert oft zusätzliche nachgeschaltete Reinigungsschritte, was die Prozesskosten erhöht.
Heterogene Katalyse
Der Katalysator befindet sich in einer anderen Phase als die Reaktanten. In der Regel ist der Katalysator ein Feststoff, während sich die Reaktanten in der Gasphase oder in einer flüssigen Phase befinden. Dieser Zustand ermöglicht ununterbrochene industrielle Prozesse, bei denen die Produkte den Reaktor verlassen können, während der feste Katalysator zurückbleibt.
Der Katalysatorträger ist bei der heterogenen Katalyse von entscheidender Bedeutung, da er den erforderlichen physikalischen Zustand, die Dimensionsstabilität und die Oberflächengeometrie bereitstellt, um anhaltende chemische Reaktionen im großen Maßstab und verschiedene chemische Prozesse zu ermöglichen.
Wichtige Eigenschaften, die die katalytische Effizienz beeinflussen
Die Auswahl der Katalysatorträgermaterialien erfolgt nicht willkürlich. Je nach den industriellen Prozessen müssen die Ingenieure eine Reihe von physikalischen und chemischen Faktoren berücksichtigen, um sicherzustellen, dass der endgültige Katalysator die Erwartungen erfüllt und die Gesamtaktivität des Katalysators aufrechterhält. Drei wichtige Faktoren bestimmen diese Leistung.
Oberfläche und Dispersion der aktiven Stelle
Der Hauptzweck eines Trägers besteht darin, die Dispersion des aktiven Metalls zu maximieren, indem die Vorteile einer größeren Oberfläche genutzt werden. Die Dispersion beschreibt die Anzahl der aktiven Metallatome an der Oberfläche im Vergleich zur Gesamtzahl der Metallatome. Träger mit großer Oberfläche (gemessen als spezifische Oberfläche in Quadratmetern pro Gramm (m²/g) nach der BET-Methode (Brunauer-Emmett-Teller)) bieten dem aktiven Metall mehr Verankerungsmöglichkeiten. Letztlich bestimmt die Oberfläche eines Katalysators sein Potenzial.
Wenn die Träger eine Oberfläche von 100 m²/g oder sogar 1000 m²/g haben, können die Hersteller eine hohe katalytische Aktivität mit geringerer Beladung mit teuren Edelmetallen erreichen. Eine hohe Dispersion ist direkt proportional zu einer hohen Umsatzfrequenz (die Anzahl der chemischen Umwandlungen pro aktiver Stelle pro Sekunde). Wenn die Prozessbedingungen zu einer Verschlechterung der Oberfläche führen, wandern die aktiven Stellen und verschmelzen, was zu einer erheblichen Verringerung der katalytischen Aktivität führt.
Porosität und Porengrößenverteilung
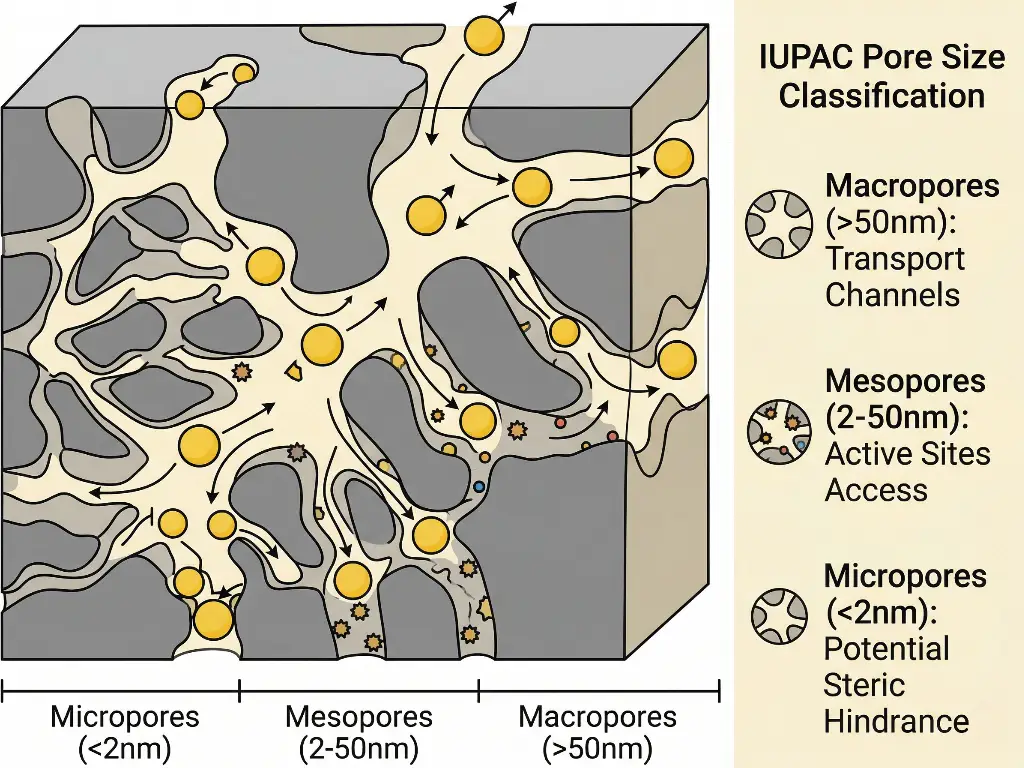
Selbst bei einer großen Oberfläche kann eine Trägerstruktur unwirksam sein, wenn ihre internen aktiven Stellen von den Reaktionsmolekülen nicht erreicht werden können; die komplexe Porenarchitektur eines Trägers diktiert den Stoffaustausch eines Katalysators. Die Reaktanten müssen durch die poröse Struktur diffundieren, mit den aktiven Stellen reagieren, und die Produkte müssen durch die poröse Struktur zurückdiffundieren und austreten.
Nach der IUPAC-Klassifikation wird die Porengrößenverteilung in drei Kategorien unterteilt:
Mikroporen
Weniger als 2 Nanometer.
Mesoporen
Zwischen 2 und 50 Nanometern.
Makroporen
Größer als 50 Nanometer.
Wenn die Porenstruktur vollständig mikroporös ist und die Reaktionsmoleküle groß sind, werden die inneren Oberflächen des Trägers durch sterische Hindernisse unzugänglich. Besteht der Träger dagegen nur aus Makroporen, ist die Diffusion zwar schnell, aber die Gesamtoberfläche und die Metalldispersion sind zu gering, um hohe Reaktionsgeschwindigkeiten zu erzielen. Daher sind bei der Entwicklung eines Katalysatorträgers die besten Katalysatorträger diejenigen mit einer Kombination von Porenstrukturen, bei denen Makroporen als Transportkanäle und mesoporöse oder mikroporöse Bereiche zur Schaffung aktiver Stellen verwendet werden. Dieses Gleichgewicht garantiert ein hohes Porenvolumen.
Mechanische Festigkeit und thermische Stabilität
Chemische Prozesse finden weit entfernt von den kleinen Bechergläsern im Labormaßstab statt, mit denen man zu arbeiten gewohnt ist. Stattdessen werden große Festbettreaktoren verwendet, die mehrere Dutzend Meter hoch sein können. Ein Katalysatorträger muss in der Lage sein, dem hydrostatischen Druck des darüber liegenden Katalysatorbetts standzuhalten. Wenn der Träger eine unzureichende Druckfestigkeit aufweist (keine ausreichende mechanische Festigkeit und keine ausreichenden allgemeinen mechanischen Eigenschaften), brechen die untersten Pellets im Reaktor auseinander und werden zu Staub. Dieser Staub sammelt sich in den Leerräumen zwischen den verbleibenden intakten Pellets an, was zu einem starken Druckabfall im Reaktor führt. Ein solches Ereignis führt zu einer ungeplanten und kostspieligen Abschaltung der gesamten Anlage.
Genauso wichtig ist die thermische Stabilität des Trägers. Viele der katalytischen Reaktionen, einschließlich Oxidation und Hydrocracking, sind exotherm. Das bedeutet, dass eine beträchtliche Wärmemenge erzeugt wird, und es ist wichtig, dass der Träger auch bei diesen hohen Temperaturen seine strukturelle Identität beibehält und neben seinem Porenvolumen und seiner Oberfläche eine hohe thermische Stabilität aufweist. Wenn das Trägermaterial schmilzt oder aufgrund der hohen Temperaturen eine Phasenänderung oder einen Strukturkollaps erfährt, verliert der Träger auch seine katalytische Aktivität.
Industrielle Anwendungen von Katalysatorträgern
Katalysatorträger werden nach den spezifischen Anforderungen der verschiedenen Branchen gebaut. Ihre spezifischen Betriebsbedingungen bestimmen, welche Materialien verwendet werden.
Petrochemische Raffinierung und Verarbeitung
Bei der petrochemischen Raffination wird Rohöl in Kraftstoffe und chemische Bausteine umgewandelt, und zwar durch Prozesse, die unter extremen Temperaturen und Drücken ablaufen, häufig in Umgebungen mit unterschiedlichem Säuregehalt. Bemerkenswerte Beispiele sind das Fluid Catalytic Cracking (FCC) und das katalytische Reforming. Die Träger in diesen Prozessen müssen schwach saure Eigenschaften aufweisen, um die Spaltung von Kohlenstoffbindungen zu fördern und die Isomerisierung einzuleiten. Aus diesem Grund werden aktiviertes Aluminiumoxid und andere technische kristalline Molekularsiebe verwendet, da sie über die erforderlichen sauren Stellen, thermischen Grenzen und mechanischen Eigenschaften verfügen, um wiederholten, kontinuierlichen Zyklen der Kohlenstoffregeneration standzuhalten, bei denen der Kohlenstoff bei einer hohen Temperatur verbrannt wird.
Kontrolle der Umweltemissionen
Aufgrund der strengen gesetzlichen Vorschriften ist die Kontrolle gefährlicher Emissionen, insbesondere flüchtiger organischer Verbindungen (VOC), Stickoxide (NOx) und Schwefeloxide (SOx), erforderlich. Bei industriellen Anwendungen wie der regenerativen katalytischen Oxidation (RCO) und Autoabgasen erleichtert der Träger schnelle Oxidations- oder Reduktionsreaktionen. Die Rolle des Katalysatorträgers ist hier entscheidend für die Haltbarkeit. Die Behandlung industrieller VOC wird bei hoher Luftfeuchtigkeit erschwert. In diesen Situationen konkurriert der Wasserdampf oft mit den VOC um die verfügbaren Adsorptionsstellen am Katalysator. In diesen Fällen werden hydrophobe (wasserabweisende) Zeolithe bei der Behandlung von industriellen VOC eingesetzt. Diese Zeolithe sind in einzigartiger Weise in der Lage, Wasser abzustoßen und gleichzeitig VOC selektiv an aktiven Metallstellen zu adsorbieren und zu konzentrieren, was eine hohe Zerstörungseffizienz in feuchten Abgasen gewährleistet.
Chemische Feinsynthese
Die Synthese von Arzneimitteln, Agrochemikalien und Spezialpolymeren umfasst komplexe, mehrstufige Reaktionen, wie selektive Hydrierungen oder Oxidationen. Bei diesen Verfahren ist eine hohe Produktreinheit von entscheidender Bedeutung. Daher müssen Nebenreaktionen strikt vermieden werden, weshalb der Katalysatorträger chemisch inert sein muss. Weist der Träger unbeabsichtigte saure oder basische Stellen auf, könnte er die Bildung unerwünschter Nebenprodukte katalysieren. In der Feinchemie werden üblicherweise Materialien mit neutralen Oberflächen - wie hochreines Kieselgel oder bestimmte Kohlenstoffmatrizen - eingesetzt, um absolute Selektivität zu erreichen.
Aufstrebende Energie und Elektrokatalyse
Elektrochemische Geräte - insbesondere Protonenaustauschmembran-Brennstoffzellen (PEMFCs) und Wasserelektrolyseure für die Erzeugung von grünem Wasserstoff - sind von zentraler Bedeutung für den Übergang zu erneuerbaren Energien. Bei diesen Anwendungen unterscheiden sich die Anforderungen an Katalysatorträger grundlegend von denen der traditionellen Thermokatalyse. Im Gegensatz zu thermokatalytischen Trägern müssen diese Materialien elektronisch leitfähig sein, um den Stromkreis zu schließen, und so beschaffen sein, dass sie extremen elektrochemischen Potenzialen in stark sauren oder basischen Flüssigphasen standhalten. Unter solch rauen Bedingungen neigen herkömmliche Metalloxide dazu, sich aufzulösen. Folglich sind leitfähige Kohlenstoffe mit großer Oberfläche, wie z. B. Kohlenstoff-Nanoröhren, und korrosionsbeständige Metalloxide (z. B. dotierte Titan- oder Tantaloxide) die erste Wahl für Elektrokatalysatorträger.
Gemeinsame Materialien zur Unterstützung von Katalysatoren

Für eine effektive technische Spezifikation ist es wichtig, die intrinsischen Eigenschaften von Materialien zu kennen. Die folgenden Materialien sind ein Beispiel für die Grundlagen der industriellen Katalysatorunterstützung. Jedes der aufgelisteten Materialien hat einzigartige physikalische und chemische Eigenschaften, die die Einsatzgrenzen festlegen, die weitgehend durch ihre allgemeine chemische Stabilität bestimmt werden.
Aktivierte Tonerde
γ-Al2O3 (Gamma-Aluminiumoxid) ist einer der weltweit am häufigsten verwendeten Katalysatorträger. Er verfügt über eine einzigartige Kombination aus großer Oberfläche (100 bis über 300 m²/g), hervorragender mechanischer Festigkeit und amphoteren Oberflächeneigenschaften (die je nach Synthese sowohl saure als auch basische Stellen enthalten). Seine thermische Stabilität macht es zur bevorzugten Wahl für Hochtemperaturanwendungen, wie z. B. Erdölraffination, Claus-Schwefel-Rückgewinnungsanlagen und Fahrzeugkatalysatoren. Darüber hinaus widersteht seine robuste physikalische Struktur hohen mechanischen Belastungen und verhindert Druckabfälle im Reaktor. Bei hohen Temperaturen (typischerweise über 800°C), insbesondere in Gegenwart von Wasserdampf, geht Gamma-Aluminiumoxid in einen Phasenübergang über α-Al2O3 (Alpha-Tonerde). Dieser Strukturkollaps führt zu einer drastischen Verringerung der Oberfläche und einer anschließenden Deaktivierung des Katalysators.
Zeolithe und Molekularsiebe
Zeolithe sind kristalline Materialien aus Aluminium und Silizium mit hoch geordneten Gerüsten aus internen Mikroporen. Im Gegensatz zu amorphen Trägern weisen Zeolithe eine hohe Einheitlichkeit mit spezifischen Porengrößen von 0,3 bis 1,0 Nanometern auf, während amorphe Träger eine zufällige, breite Verteilung der Porengrößen aufweisen. Aufgrund dieser Gleichförmigkeit und mikroskaligen Präzision verfügen Zeolithe über eine spezielle Form der Katalyse, die "formselektive Katalyse". Bei diesen Materialien haben nur Reaktanten, die kleiner als die Porengröße des Zeoliths sind, Zugang zu den internen katalytischen Stellen, und nur bestimmte Produkte können den Katalysator verlassen und zur nächsten Stufe der Katalyse übergehen. Darüber hinaus sind Zeolithe sehr begehrt, weil es möglich ist, durch Modifizierung der Synthese eines Zeoliths und Steuerung des Si/Al-Verhältnisses Zeolithe mit einer bestimmten Oberflächenazidität zu erhalten, die von leicht bis stark sauer reicht. Diese Eigenschaft von Zeolithen macht sie äußerst wertvoll für das katalytische Fließbettcracken und die komplexe Isomerisierung.
Kieselgel (SiO2)
Kieselgel, eine amorphe und hochporöse Art von Siliziumdioxid, hat eine insgesamt neutrale Oberfläche und liefert durchgängig über 200 m²/g bis zu 800 m²/g Oberfläche. Bei der Herstellung von Katalysatoren bietet die präzise Kontrolle der inneren Porenstruktur während der Sol-Gel-Synthese den größten Nutzen. Darüber hinaus entwerfen die Ingenieure Silikat-Träger mit sehr spezifischen Meso- und Makroporengrößen, die den Durchgang großer Reaktionsmoleküle ermöglichen. Aufgrund seiner völlig inerten Eigenschaften wird Siliciumdioxid häufig als Träger für aktive Metalle gewählt, wenn Säure- oder Basenstellen unerwünschte Polymerisationen, Risse oder Umlagerungen der Reaktanten verursachen würden. Der größte Nachteil ist die fehlende hydrothermale Stabilität, da sich das Silica-Gerüst bei hohen Temperaturen und hoher Feuchtigkeit zersetzt.
Aktivkohle-Materialien
Verschiedene Formen von Kohlenstoff, darunter Aktivkohle, Ruß und technisch hergestellte Kohlenstoff-Nanoröhren, haben spezifische Oberflächen, die 1000 m²/g übersteigen können. Die einzigartige Struktur von Kohlenstoff ermöglicht eine Reihe von Eigenschaften, darunter eine intrinsische elektrische Leitfähigkeit und eine hohe Widerstandsfähigkeit gegen chemische Angriffe in stark sauren und stark basischen Umgebungen. Aus diesem Grund dient Kohlenstoff als wesentliches Substrat für die Einbindung von Edelmetallen (d. h. Platin, Palladium und Ruthenium) bei der Flüssigphasenhydrierung, der Edelmetallrückgewinnung und der modernen Elektrokatalyse. Allerdings haben Kohlenstoffträger einen grundlegenden Nachteil: ihre mangelnde thermische Stabilität in oxidierenden Umgebungen. Bei Temperaturen über 400 °C verbrennt der Kohlenstoffträger und das gesamte Katalysatorbett geht verloren.
Keramiken und Monolithen
Wenn eine industrielle Anwendung starke und schnelle Temperatur-, Gasdurchfluss- und Druckschwankungen erfordert, sind herkömmliche Partikelträger (Pellet- und Perlenträger) aufgrund der konstruktiven Beschränkungen unwirksam. In diesen Fällen werden Monolithen aus Keramik, insbesondere Strukturen aus Cordierit, verwendet. Diese Monolithen bestehen aus mehreren parallelen, geraden Gasströmungskanälen. Aufgrund des geringen Wärmeausdehnungskoeffizienten von Cordierit sind Monolithen aus diesem Material thermoschockbeständig. Obwohl der nackte keramische Monolith eine extrem geringe Oberfläche aufweist (in der Regel < 2 m²/g), wird auf die Kanalwände ein Washcoat aus einem hochporösen Material (in der Regel aktiviertes Aluminiumoxid) aufgetragen, um die Oberfläche zu vergrößern und die Wechselwirkung der Strömung mit dem Washcoat zu verbessern. Anschließend wird das aktive Metall auf diese Beschichtung aufgebracht. Dies ist die typische Konfiguration, wie sie in Autokatalysatoren und in den Emissionskontrollsystemen großer Kraftwerke anzutreffen ist.
Titandioxid und Zirkoniumdioxid
Titan- und Zirkoniumdioxide (TiO2 und ZrO2) sind spezielle Übergangsmetalloxid-Träger. Obwohl ihre Basisoberflächen im Allgemeinen etwas geringer sind als die von Standard-Aluminiumoxid oder Siliziumdioxid, werden sie für einen ganz bestimmten Zweck verwendet, nämlich um ein chemisches Phänomen zu nutzen, das als starke Metall-Träger-Wechselwirkung (SMSI) bekannt ist. Unter bestimmten Bedingungen eines Reduktionsprozesses wird ein Teil der Oberfläche dieser Oxide teilweise reduziert, und der Träger erfährt eine physikalische Migration, die die aktiven Metallnanopartikel teilweise einkapselt. Diese Art der physikalischen Verkapselung verändert die elektronischen Zustände und die Chemisorptionseigenschaften des aktiven Metalls drastisch, was zu einer deutlichen Verbesserung seiner katalytischen Aktivität und Selektivität für bestimmte Reaktionswege führen kann. Dies ist von großer Bedeutung für die industrielle Photokatalyse, die selektive CO-Hydrierung und die spezifische Synthesegasumwandlung.
Wie Sie die richtige Unterstützung wählen
Bei der Auswahl des richtigen Katalysatorträgers müssen die genauen thermodynamischen, chemischen und physikalischen Bedingungen des industriellen Prozesses mit den intrinsischen Eigenschaften des Trägermaterials abgestimmt werden. Die Verwendung von Materialien "wie sie sind" ohne Untersuchung der Prozessbedingungen führt unweigerlich zum Versagen des Katalysators. Der richtige Einsatz von Katalysatorträgern stellt grundsätzlich sicher, dass der Katalysator effizient arbeitet.
Die folgende Tabelle enthält eine Zusammenfassung der Vergleichsparameter der wichtigsten Trägermaterialien, die in die technischen Spezifikationen einfließen werden:
| Material Typ | Typische Oberfläche (m²/g) | Thermische Stabilität | Oberflächen-Säure/Basizität | Industrieller Schlüsselvorteil | Primäre Einschränkung |
|---|---|---|---|---|---|
| Aktivierte Tonerde | 100 - 300 | Ausgezeichnet (bis zu 800°C) | Amphoterisch | Hohe Druckfestigkeit, universelle Einsetzbarkeit in Hochtemperaturprozessen. | Unterliegt bei extremen Temperaturen einem Phasenübergang (γ zu α). |
| Zeolithe / Molekularsiebe | 300 - 1000+ | Gut bis Ausgezeichnet | Hochgradig abstimmbar (meist säurehaltig) | Präzise Formselektivität, strenge Kontrolle der Porengröße, hochaktive Säurestellen. | Anfällig für Mikroporenverstopfung durch schwere Kohlenwasserstoffe oder Verkokung. |
| Kieselgel | 200 - 800 | Mäßig | Neutral | Chemisch inert, verhindert Nebenreaktionen in der feinchemischen Synthese. | Geringere hydrothermale Stabilität im Vergleich zu Aluminiumoxid. |
| Aktivkohle | 800 - 1500+ | Schlecht (in Sauerstoff) | Neutral / Inert | Ausgezeichnete chemische Beständigkeit gegenüber aggressiven Säuren/Basen, hohe elektrische Leitfähigkeit. | Verbrennt an der Luft bei erhöhten Temperaturen. |
| Keramische Monolithen | < 2 (Waschanstrich erforderlich) | Außergewöhnlich | Neutral | Nahezu keine thermische Ausdehnung, übersteht massive Temperaturschocks, geringer Druckabfall. | Erfordert komplexe Waschbeschichtungsschritte, um die erforderliche Oberfläche zu schaffen. |
| Titandioxid / Zirkoniumdioxid | 10 - 100 | Gut | Mild säuerlich | Weist eine starke Metall-Träger-Wechselwirkung (SMSI) auf und fördert spezifische Reaktionswege. | Höhere Materialkosten, naturgemäß geringere Grundfläche. |
Um diese Daten produktiv zu nutzen, sollten Sie die branchenspezifische Anwendung strukturiert analysieren.
- Bestimmen Sie die Temperatur und die Atmosphäre: Bei Prozessen über 500°C in einer Sauerstoffumgebung (z.B. Abgasbehandlung) müssen Kohlenstoffkomponenten ausgeschlossen werden. Aktivierte Tonerde und Cordierit-Monolithen sind hier die optimale Wahl.
- Bestimmen Sie den Bedarf an Selektivität: Für Reaktionen, bei denen Moleküle getrennt werden müssen, die sich nur um den Bruchteil eines Nanometers unterscheiden (dazu gehören die Isomerisierung von Xylol und bestimmte Gasreinigungen), ist Zeolith praktisch die Standardwahl. Der Grund dafür sind die besonderen kristallinen Porengrößen.
- Bestimmen Sie die chemische Umgebung: Bei Katalysatoren, die in stark ätzender flüssiger Säure arbeiten (wie in einigen Elektrolyseuren), lösen sich Aluminiumoxid und Siliziumdioxid auf. Daher besteht die Wahl zwischen Kohlenstoff und ganz bestimmten Metalloxiden, um eine robuste Struktur zu gewährleisten.
- Bestimmen Sie das Nebenproduktrisiko: Bei Einsatzstoffen, die empfindliche Moleküle enthalten, die dazu neigen, leicht an sauren Stellen zu polymerisieren, sollten stark saure Zeolithe oder amphotere Tonerden vermieden werden. Stattdessen wird inertes Siliziumdioxid empfohlen, um die Bildung von Nebenprodukten zu minimieren.
Fehlerbehebung bei der Deaktivierung von Katalysatoren
Katalysatoren werden im Laufe industrieller Prozesse allmählich deaktiviert, wodurch die Integrität des Katalysatorträgers in Frage gestellt wird. Selbst wenn sie anfangs die Leistungsspezifikationen erfüllen, müssen Ingenieure, sobald eine Deaktivierung auftritt, die Ursache ermitteln, um anpassungsfähigere Trägermaterialien vorzuschlagen und so die Ausfallzeiten des Katalysators zu verringern.
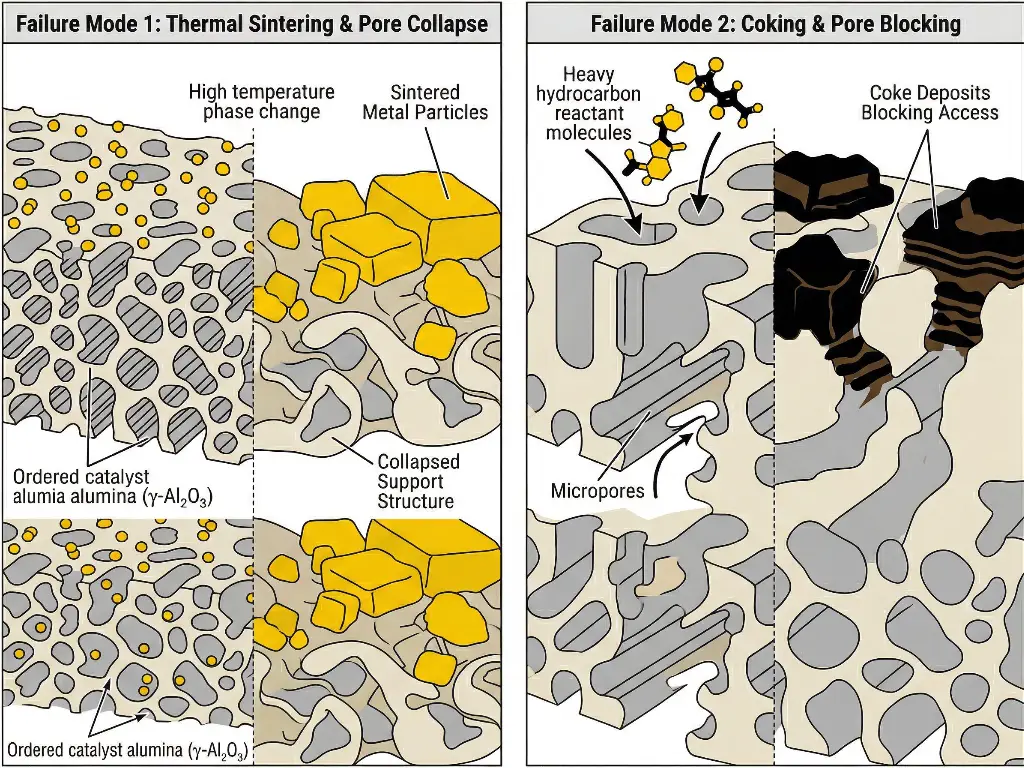
Thermisches Sintern und Porenkollaps
Ein Versagen tritt ein, wenn die thermische Belastung die festgelegten Auslegungsgrenzen überschreitet und zum Zusammenbruch der inneren Porenwände führt. Dies führt zu einem drastischen mikroskaligen Zusammenbruch der inneren Oberflächen. Bei aktiviertem Aluminiumoxid wird dies als irreversibler Phasenwechsel von der Gamma-Phase mit großer Oberfläche zur Alpha-Phase mit geringer Oberfläche beobachtet. Mit abnehmender Oberfläche kollabieren die aktiven Partikel und agglomerieren zu großen, inaktiven Partikeln.
Verkokung und Verschmutzung
Bei der Reaktion von schweren Kohlenwasserstoffen führen Nebenreaktionen zur Bildung von Koks, der sich auf den inneren Oberflächen des Trägers ablagert. Bei vollständig mikroporösen Materialien wie den klassischen Zeolithen verstopfen diese Ablagerungen schnell die Eingänge zu den Poren und verwehren den Reaktanten den Zugang zu den aktiven Stellen im Inneren der Kristalle vollständig.
Aktive Metallauswaschung
Das aktive Metall wird vom Träger abgelöst und fließt mit dem flüssigen Reaktantenstrom ab. Dies kann geschehen, weil die Haftung des Metalls auf dem Träger zu schwach ist oder der Träger selbst sich unter den Reaktionsbedingungen langsam auflöst und das Metall mit sich führt.
Schlussfolgerung und nächste Schritte
Die Spezifikation eines Katalysatorträgers ist eine wichtige technische Entscheidung, die die Effizienz der Anlage, die Produktreinheit und die Betriebszeit des Reaktors bestimmt. Ob es darum geht, die Dispersion von Platin zu maximieren, dem thermischen Kollaps in einer Oxidationseinheit zu widerstehen oder die präzise Formselektivität eines Zeolithgerüsts zu nutzen, die richtigen physikalischen und chemischen Eigenschaften des Trägers müssen perfekt auf die Prozessbedingungen abgestimmt sein. Werden Faktoren wie Porenverteilung, Druckfestigkeit oder Säuregehalt der Oberfläche nicht berücksichtigt, führt dies unweigerlich zu schneller Verkokung, Versinterung und katastrophalem Druckabfall.
Für Betriebe, die ihre katalytischen Prozesse optimieren, die Deaktivierung abmildern oder hochspezialisierte Gastrennungssysteme entwickeln wollen, ist die Zusammenarbeit mit einem erfahrenen Hersteller unerlässlich. JALON verfügt über 28 Jahre Branchenerfahrung, ein engagiertes Team von 91 Experten und eine Reihe von fortschrittlichen Analysegeräten zur Lösung komplexer Adsorptions- und Katalysatorprobleme. Mit vollautomatischen Produktionsanlagen in China und Thailand bietet JALON eine sichere, weltweit zertifizierte Lieferkette ohne Mindestbestellmengen (MOQ).
Wenn Sie herausfinden möchten, wie optimierte aktivierte Tonerde oder maßgeschneiderte Zeolith-Molekularsiebe Ihre Prozessausbeute verbessern können, wenden Sie sich noch heute an unser Ingenieursteam, um einen kostenlosen Projektanalysebericht, eine individuelle Rezepturberatung und umfassende Mustertests zu erhalten.









